Crioconservación: Mantener órganos enteros a temperaturas bajo cero para futuros trasplantes ya es posible

Mientras los biólogos del envejecimiento y los científicos del aprendizaje automático trabajan duro para desarrollar relojes biológicos del envejecimiento y formas de invertirlos, sus avances podrían no llegar a tiempo para muchos de nosotros. Por eso muchos científicos de alto nivel se están aventurando en un campo alternativo: detener los procesos degenerativos utilizando diversas tecnologías convergentes en criobiología. La mayoría de los relojes dejan de funcionar a temperaturas muy bajas. Y algunas de estas tecnologías están más cerca de la realidad de lo que usted cree. De hecho, muchas de las personas nacidas mediante fecundación in vitro (FIV), fueron crioconservadas en su día como embriones. Y los recientes avances en la crioconservación de órganos son asombrosos.
En su artículo de portada, el número actual de Science habla de un diluvio de avances sin precedentes en la crioconservación de órganos, algunos de los cuales se anunciaron recientemente en dos de las mayores conferencias anuales en el campo del trasplante de órganos: la reunión de la Asociación de Organizaciones de Obtención de Órganos, que este año celebró su 40 aniversario, y el Congreso Americano de Trasplantes.
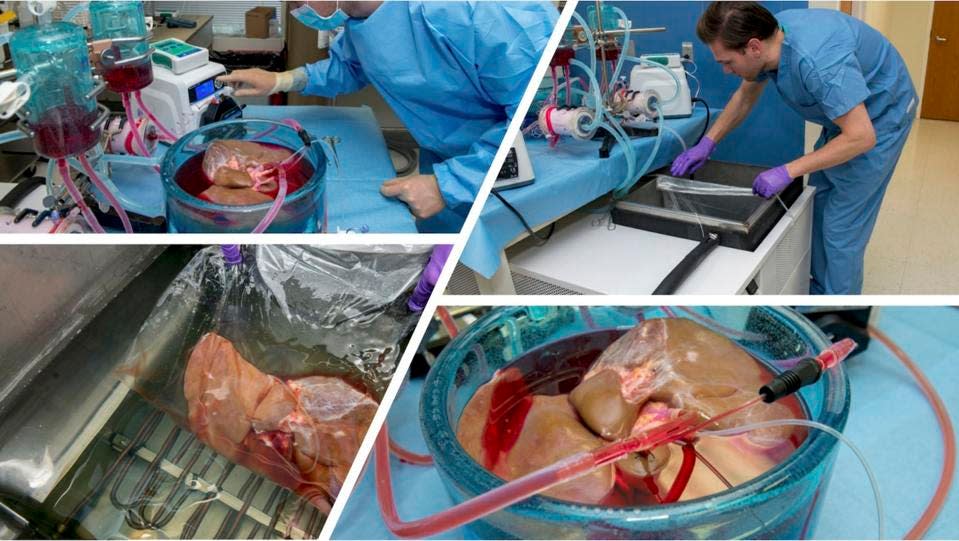
En el Congreso Americano de Trasplantes, investigadores de la Facultad de Medicina de Harvard, el Hospital General de Massachusetts y la empresa de biotecnología Sylvatica Biotech informaron de los primeros hígados humanos que se conservaron a temperaturas bajo cero durante más de 3 días, aproximadamente 10 veces el periodo de conservación clínicamente aceptable con métodos convencionales.
Scientists are learning how to cryopreserve living tissues, organs, and even whole organisms, then bring them back to life.
Learn more in the latest issue of Science: https://t.co/dleC8LcFDP pic.twitter.com/fHmZobpT5T— Science Magazine (@ScienceMagazine) June 29, 2023
El informe sigue al reciente estudio del mismo grupo de investigación en Nature Biotechnology en el que se informaba del primer almacenamiento con éxito de hígados humanos a temperaturas bajo cero, que fue ampliamente cubierto por publicaciones como JAMA y The Atlantic y aclamado por el director de los Institutos Nacionales de Salud de EE.UU. como un avance significativo en este campo.
Mientras tanto, un grupo de investigación de Johns Hopkins que trabaja con Sylvatica Biotech informó del éxito del trasplante de extremidades de mamíferos tras 3 días de almacenamiento a temperaturas bajo cero. Si el enfoque de la conservación de extremidades puede ampliarse a los seres humanos como se ha hecho con el del hígado, podría ayudar a desbloquear la estancada práctica del trasplante de extremidades. Encontrar una compatibilidad estrecha entre donantes y receptores puede ser un reto mucho más extremo para el trasplante de extremidades, manos o cara que para el de órganos internos. Con la capacidad de enviar este tipo de trasplantes a través de un continente o de todo el mundo, podrían ser factibles órdenes de magnitud más de estos trasplantes.
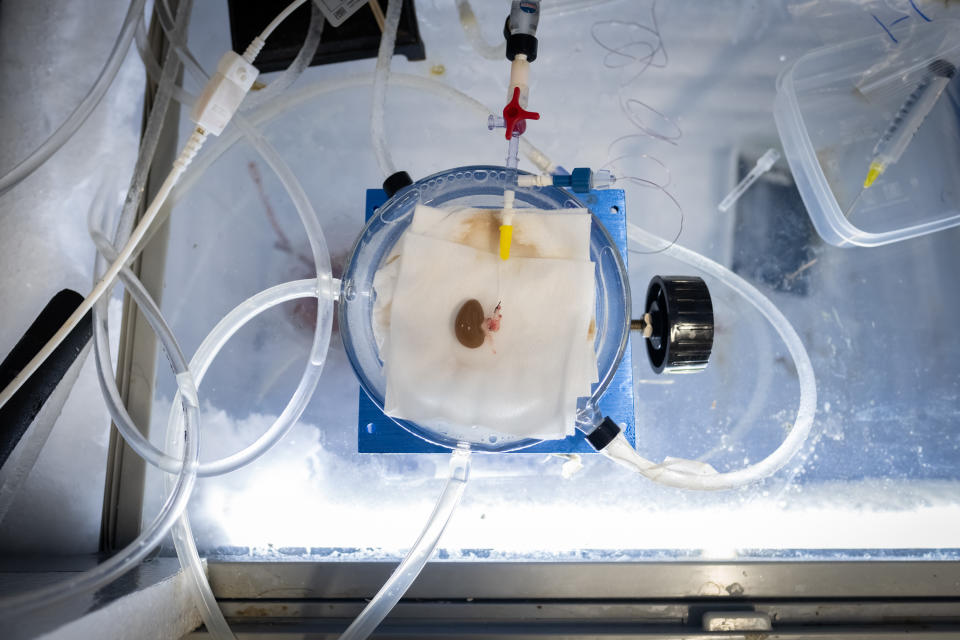
Más tarde, en la reunión de la Asociación de Organizaciones de Obtención de Órganos, en una sesión plenaria de estreno a cargo del CEO de Sylvatica Biotech y del director del programa de crioconservación ATP-Bio de la Fundación Nacional de la Ciencia, se anunció el primer procedimiento con éxito para almacenar órganos de mamíferos para trasplante a temperaturas criogénicas profundas. Se había publicado en Nature Communications sólo unos días antes. La publicación abre la puerta al almacenamiento de órganos para trasplantes del mismo modo que hoy se almacenan óvulos y embriones para la fecundación in vitro. A efectos de demostración, los riñones del estudio se habían mantenido a temperaturas criogénicas profundas (inferiores a -140℃) hasta 100 días antes de calentarlos a la temperatura corporal y trasplantarlos a ratas. Este estudio es revolucionario y espero tratarlo en otro artículo.
A estas temperaturas los órganos podrían teóricamente almacenarse durante años e incluso muchos siglos sin que se produjera ningún cambio medible a nivel molecular. Los órganos quedaron congelados en el tiempo. Se trata de un momento decisivo en el campo de la crioconservación, y en décadas futuras puede que se recuerde como la demostración fundamental de que los órganos pueden almacenarse fuera del cuerpo durante un tiempo ilimitado.
En los últimos números he cubierto el renacimiento emergente de la criopreservación y el trabajo del grupo del Dr. Dayong Gao. Los anuncios de este mes pueden ser la señal más clara de que el campo ha alcanzado la mayoría de edad.
Para entender cómo se ha llegado a este punto, he profundizado en la carrera del fundador y CEO de Sylvatica Biotech, el Dr. Sebastian Giwa (llamado "Seb" por sus amigos). Muchos consideran a Seb el principal artífice del auge del interés científico por la crioconservación en los últimos años.
Seb presume de un currículum increíblemente largo para alguien que sólo lleva una década trabajando en este campo. Entre otros éxitos empresariales, es el fundador de varias empresas diferentes en el espacio que han crecido y prosperado, entre ellas la organización sin ánimo de lucro Organ Preservation Alliance y las empresas de utilidad pública Ossium Health y Sylvatica Biotech. Seb también es cofundador de otras iniciativas importantes, como el Instituto de Investigación Biostasis y una nueva rama de la Sociedad Americana de Trasplantes, y forma parte del consejo de administración de NDN (Nevada Donor Network), una de las organizaciones estadounidenses con más éxito encargada de gestionar la donación de trasplantes de órganos.
Seb es el presidente fundador de Expanse Bio y de ATP-Bio Partners, el consorcio industrial del programa nacional de investigación en criopreservación de la Fundación Nacional de la Ciencia de EE UU. Recientemente formó parte de una corta lista de líderes biotecnológicos (junto a otros como Bill Gates, George Church y J. Craig Venter) a los que la preeminente revista científica Nature Biotechnology recurrió con motivo de su 25 aniversario para que describieran las áreas en las que las ciencias de la vida harán el mayor impacto en la sociedad en los próximos años.
Resulta que el renacimiento de la criopreservación no es un accidente; lleva una década haciéndose. Y según Seb y otras personas con las que hablé, la crioconservación está a punto de cambiar para siempre el trasplante de órganos. ¿Y después? Toda la salud humana.
¿Puede la crioconservación solucionar la escasez de órganos?
En la mañana del estreno de la 40ª reunión anual de la Asociación de Organizaciones de Obtención de Órganos ("AOPO"), Seb dirigió una sesión plenaria sobre la crioconservación de órganos. Se presentaron los nuevos logros ante un auditorio abarrotado, pero no era el público habitual de una charla científica: en lugar de investigadores, la audiencia estaba compuesta principalmente por ejecutivos de organizaciones de obtención de órganos ("OPO", por sus siglas en inglés). Estas organizaciones sin ánimo de lucro tienen la misión, encomendada por el gobierno estadounidense, de coordinar todas las donaciones de órganos dentro de sus respectivas regiones geográficas (normalmente del tamaño de un estado de EE.UU.), colaborando con los hospitales locales para identificar a los posibles donantes y ofreciendo después esas donaciones a los pacientes de la lista nacional de espera para trasplantes.

Durante los últimos años, algunas OPO han estado muy implicadas en los esfuerzos para aumentar la financiación de la criopreservación de órganos, incluso ayudando a persuadir a la Fundación Nacional de la Ciencia de EE.UU. para que establezca un programa nacional de investigación en criopreservación. Un aspecto inusual del avance en criopreservación renal que se presenta en la AOPO es que cinco de estas OPO habían financiado personalmente el estudio, igualando subvenciones de agencias científicas estadounidenses. Varias OPO también habían estado proporcionando un suministro constante de órganos de donantes rechazados (no trasplantados) para los estudios de crioconservación, ayudando a salvar la distancia entre la prueba de concepto animal y los datos humanos mucho más rápido de lo que cabría esperar en un programa típico de investigación médica.
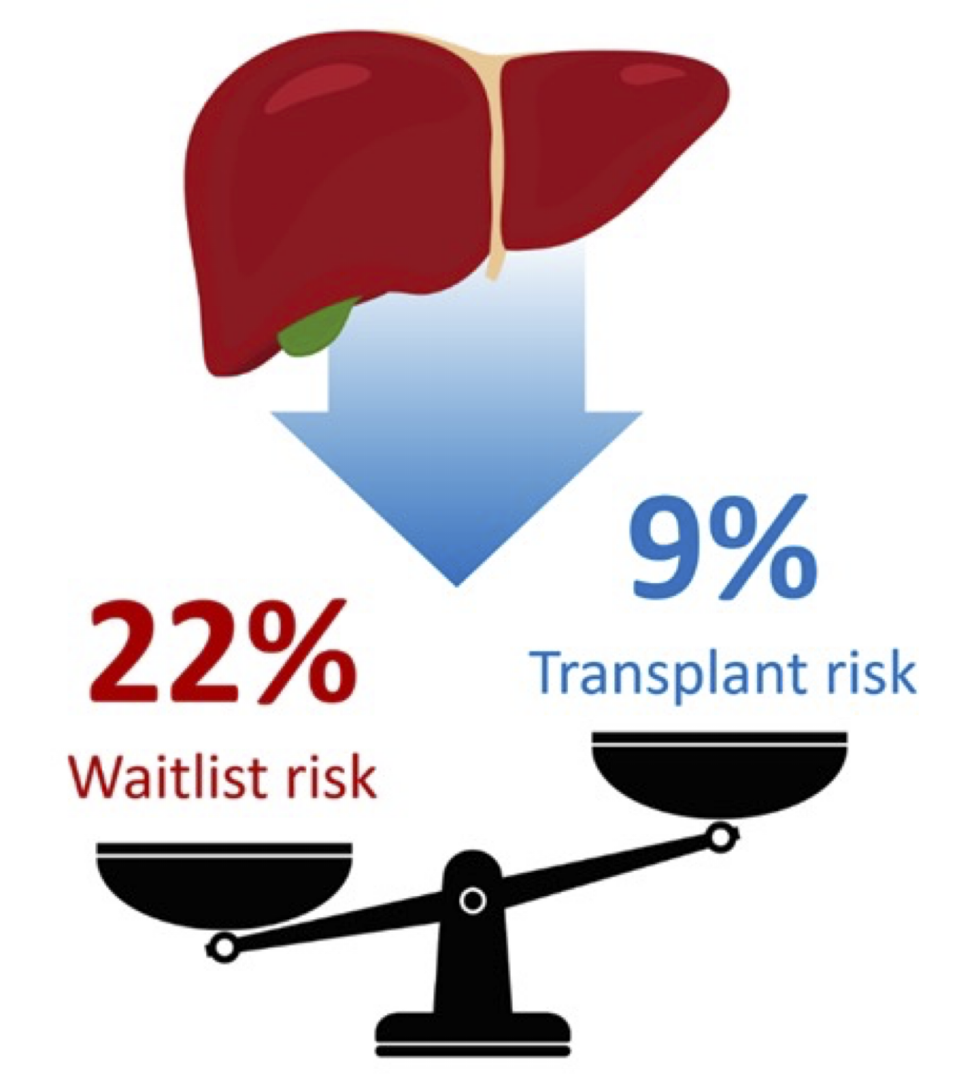
Las OPO tienen buenas razones para interesarse por la crioconservación de órganos. A pesar de los doce años consecutivos de aumento récord de trasplantes realizados, la mayoría de las ofertas de órganos de las OPO estadounidenses son rechazadas por los centros de trasplante cercanos. Por ejemplo, en EE.UU. un paciente que muere esperando un nuevo hígado ha tenido una mediana de 6 ofertas de hígado de donante rechazadas en su nombre por su programa de trasplantes.
Se ha rechazado una mediana de 16 ofertas por cada paciente que fallece en la lista de espera de riñón. La mayoría de los pacientes nunca llegan a saber que se ha hecho una oferta. Incluso los niños que necesitan un trasplante de corazón, que se encuentran entre los receptores más difíciles de emparejar con los donantes, experimentan algo similar. La gran mayoría recibe una oferta aceptable, y el equipo de trasplantes la rechaza en un 85% de las ocasiones. Muchos de estos hígados, riñones y corazones caducan antes de ser aceptados por algún centro de trasplantes lo suficientemente cercano como para aceptarlos. Los estudios sugieren que muchos (si no la mayoría) de esos órganos son realmente trasplantables y habrían beneficiado a los pacientes.

Este problema se puso de manifiesto el año pasado en un informe de las Academias Nacionales de Ciencias, Ingeniería y Medicina (NASEM). El estudio de la NASEM fue provocado en parte por las afirmaciones a menudo citadas de que la causa principal de la escasez de órganos es una simple falta de oferta: un fallo de las OPO a la hora de identificar suficientes donantes adecuados y facilitar ofertas para trasplantes. Pero el informe de la NASEM concluyó que la situación es mucho más compleja que eso. Dentro de tiempos y geografías localizadas, las OPO ofrecen con frecuencia más órganos trasplantables de los que aceptan los centros de trasplante cercanos.
El trasplante de órganos puede ser uno de los logros más profundos y significativos de la civilización humana hasta la fecha, pero un órgano fuera del cuerpo sigue compartiendo algunas limitaciones directas con otras cosas que caducan rápidamente. Intentar donar órganos (sin crioconservación) se parece mucho a intentar donar alimentos perecederos (no enlatados): sin duda hay mucha gente hambrienta en el mundo, pero buena suerte encontrando un receptor para cada onza antes de que caduque. Cada vez hay más pruebas de que si estos órganos pudieran ofrecerse a más pacientes, y especialmente a pacientes de programas de trasplante más alejados de la OPO que ofrece el órgano, muchos de ellos serían aceptados.
Un factor crucial es que la población de donantes de órganos es notablemente heterogénea. Cada donante tiene un historial médico único, y docenas de factores pueden influir en los riesgos y beneficios de trasplantar un órgano concreto a un determinado paciente en lista de espera. No existe una línea clara entre los órganos "trasplantables" y los que no lo son. El conjunto de órganos que teóricamente podrían trasplantarse (proporcionando un beneficio de supervivencia y mejorando la calidad de vida del receptor) es al menos varias veces superior al que se trasplanta hoy en día.
Pero a medida que los centros de trasplantes "profundizan" en esa reserva, trasplantando órganos de donantes con más complicaciones médicas, se espera que esos órganos conlleven un mayor riesgo de fracaso del trasplante, rechazo del órgano y otros efectos secundarios adversos. Aunque la mayoría de esos trasplantes siguen teniendo éxito, la esperanza de vida de los pacientes tras el trasplante suele disminuir a medida que los centros de trasplantes profundizan en la reserva de donantes. Esto significa que, para un programa de trasplantes, una de las decisiones más importantes es si aceptar un órgano que se ofrece hoy o esperar a ver si llega una oferta "mejor" antes de que sea demasiado tarde.
Cada centro de trasplantes tiene una dotación única de experiencia práctica y juicio sobre qué ofertas de órganos aceptar para sus pacientes. Sus prácticas de aceptación de órganos también se ven influidas por las circunstancias únicas de cada centro, como las poblaciones de pacientes que atienden, las limitaciones logísticas e incluso los riesgos normativos y financieros. Algunos centros de trasplantes aceptan ofertas de órganos más diversas que otros, y estas diferencias específicas de cada programa abarcan los principales órganos de trasplante (hígados, corazones, pulmones y riñones). Las disparidades pueden ser extremas: algunos centros pueden aceptar una gama mucho más amplia de ofertas de las OPO sin comprometer los resultados para sus pacientes.
La variación es aún más sorprendente si se compara EE.UU. con otros países. Por ejemplo, aunque España y EE.UU. compiten anualmente por la distinción de realizar el mayor número de trasplantes de órganos de donantes fallecidos per cápita del mundo (ningún otro país se le acerca), en España muchas más de estas donaciones proceden de donantes mayores de 70 años. Los centros de trasplantes estadounidenses suelen presumir que estos órganos de más edad son de menor calidad.
Estas disparidades regionales y globales contribuyen en gran medida a la escasez de órganos. Por ejemplo, un estudio reciente comparó las prácticas de aceptación de riñones de los centros de trasplantes de Francia con las de EE.UU. y utilizó esta información para elaborar un modelo del número de riñones estadounidenses que habrían sido aceptados por los centros de trasplantes franceses basándose en el historial médico del donante. Descubrieron que el 62% de los riñones de desecho estadounidenses se habrían trasplantado en Francia, lo que habría supuesto más de 130.000 años de vida agregados que se habrían añadido durante el periodo de diez años del estudio si las OPO estadounidenses hubieran podido ofrecer esos riñones a los programas de trasplante que utilizan las prácticas francesas de aceptación de órganos.
Durante décadas se han propuesto soluciones políticas para mitigar este problema, pero su eficacia tiene un límite. Aunque un paciente y su familia pueden elegir donar, su hospital puede notificarlo a la OPO, la OPO puede ofrecer órganos a los pacientes de los centros de trasplantes y una lista de espera nacional puede decidir quién recibe primero la oferta de órganos... nadie puede obligar a un cirujano a aceptar el órgano que se le ofrece y trasplantarlo a su paciente. Es crucial que cada programa de trasplantes actúe como defensor del paciente individual, lo que significa que deben tener en cuenta que mañana podría llegar una oferta de órgano "mejor". Cuantos más órganos de donantes ofrezca una OPO, más selectivos estarán incentivados a ser los centros de trasplantes cercanos.
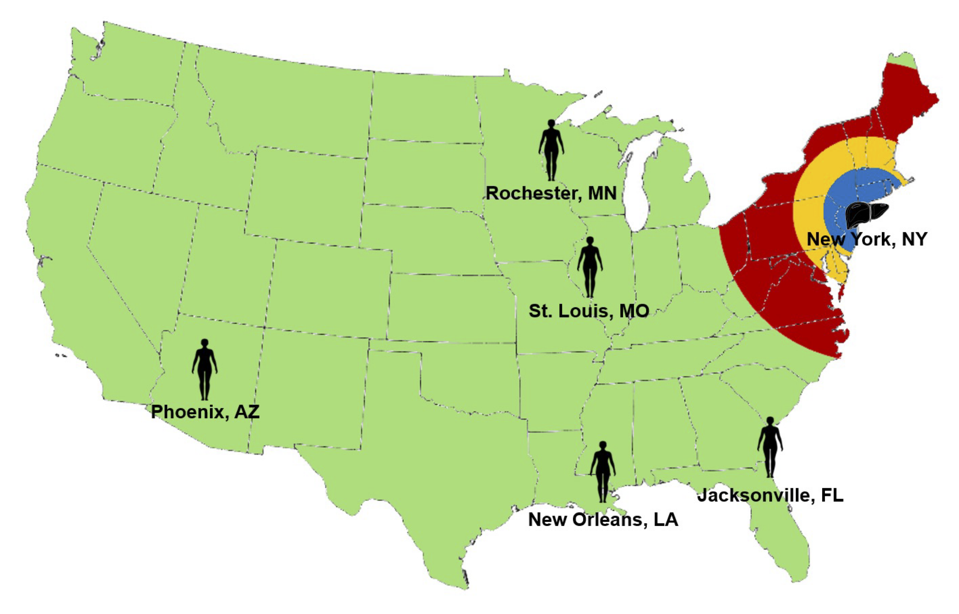
El informe de la NASEM señalaba que las variaciones en las prácticas de aceptación de los centros de trasplante cercanos repercuten directamente en el rendimiento de las OPO, lo que agrava la escasez de órganos. Otros estudios han identificado este fenómeno para los trasplantes de hígado, corazón, pulmón y riñón. Esto significa que un factor determinante del éxito es la proximidad de las OPO a programas de trasplante que estén dispuestos y sean capaces de aceptar órganos con una gama más amplia de características médicas. Dado que hoy en día los órganos que se encuentran fuera del cuerpo caducan en cuestión de horas, muchos de los que se donan demasiado lejos de estos centros de trasplante se convierten en oportunidades perdidas para salvar a pacientes.
Varias OPO trabajan ahora con Sylvatica Biotech para resolver este talón de Aquiles del sistema de trasplantes estadounidense, desarrollando el método de crioconservación de hígados como forma de ofrecer hígados de donantes a una distancia y un tiempo mucho mayores. El objetivo: desligar a la OPO de su geografía y de las circunstancias locales.
Para entender lo que esto podría significar para la escasez de órganos hablé con Jedd Lewis, CEO de la organización sin ánimo de lucro Organ Preservation Alliance. Jedd es también el presidente fundador de la Comunidad de Práctica de Recuperación y Preservación de la Sociedad Americana de Trasplantes y miembro del consejo asesor de Sylvatica. Le pregunté cuántos trasplantes de hígado más podrían derivarse de las tecnologías de Sylvatica. Su respuesta: los factores en juego son complejos, pero en las condiciones adecuadas el potencial es nada menos que miles de trasplantes de hígado adicionales que salven vidas cada año procedentes de donantes estadounidenses. Teniendo en cuenta que hoy en día se realizan menos de 10.000 trasplantes de hígado al año en EE.UU., el impacto sobre la escasez de órganos sería profundo.
Esta situación dista mucho de las perspectivas de los trasplantes hace una década. En aquel momento, la crioconservación de órganos era un subcampo oscuro que había quedado huérfano en su mayor parte tanto para los financiadores como para la comunidad científica. Para muchos, la perspectiva de una conservación ilimitada de órganos era una fantasía.
¿Cómo hemos llegado hasta aquí?
Un "Programa Apolo" en Criopreservación de Órganos
En el verano de 2012, Seb formó parte de una pequeña fracción de empresarios, científicos y médicos admitidos en el Programa de Soluciones Globales en el campus de la NASA en Silicon Valley ("GSP" para abreviar). El programa formaba parte de la Singularity University, que se había puesto en marcha como una colaboración entre organizaciones como Google, la NASA, Genentech, Cisco y un grupo de futuristas de alto perfil, entre ellos Peter Diamandis y Ray Kurzweil, con la misión de "preparar a la humanidad para un cambio tecnológico acelerado." Los estudiantes del SPG tuvieron un acceso envidiable a científicos e ingenieros de gran prestigio. Estos expertos les impartieron un curso intensivo sobre una amplia gama de tecnologías que avanzan exponencialmente, como la robótica, la nanotecnología, la ingeniería genética y la inteligencia artificial. A continuación, se pidió a los estudiantes que encontraran nuevas formas de aprovechar estas tecnologías para resolver los "grandes retos" de la humanidad, como el hambre, la contaminación y las enfermedades. El mandato era audaz, pero directo: influir positivamente en al menos 1.000 millones de personas.
Tras barajar cientos de ideas con sus compañeros de clase, Seb se centró en un área relativamente oscura de la tecnología que había sido cubierta en el programa SPG: la crioconservación. El concepto en sí era inmensamente poderoso. ¿Qué pasaría si pudiéramos almacenar seres vivos, como órganos para trasplantes y tejidos vivos para la investigación, del mismo modo que hoy podemos almacenar alimentos, datos, energía y otros recursos? Esto podría hacer que la salud humana sufriera la misma transformación que habían sufrido esas otras industrias. Esto ya había ocurrido al menos dos veces: la primera, la crioconservación de líneas celulares humanas a mediados del siglo XX, había permitido gran parte de la investigación médica moderna. Después, la crioconservación de ovocitos y embriones en la década de 1980 había transformado la salud reproductiva al facilitar la fecundación artificial.
Sin embargo, la crioconservación no era exactamente una tecnología de "avance exponencial". Mientras que las células y los embriones eran posibles de crioconservar debido a su pequeño tamaño, el almacenamiento criogénico de tejidos más grandes y órganos enteros era a menudo descartado por los expertos como imposible. Sólo un puñado de laboratorios de investigación en el mundo trabajaban en el problema y el interés de los organismos de financiación era inexistente. Así que Seb propuso algo fuera de lo común incluso para los estándares del SPG: mientras todos los demás estudiantes creaban empresas emergentes futuristas de "tecnología profunda", Seb estableció un grupo de defensa de la ciencia en el molde de la Sociedad Americana del Cáncer. Convenció a varios otros estudiantes de SPG para que se unieran a él, y así nació la Alianza para la Preservación de Órganos ("OPA", por sus siglas en inglés). Más tarde, cuando el cofundador de la Singularity University (SU), Peter Diamandis, describió siete de las empresas más interesantes y emocionantes surgidas de la SU, nombró a OPA como una de ellas.
Seb tenía unos antecedentes poco probables para impulsar un área estancada de la ciencia. Se había doctorado en la Escuela de Economía de Estocolmo, en Suecia, y después emigró a EE.UU. para seguir una carrera en finanzas. Tras graduarse entre el 5% de los mejores de su clase en la Harvard Business School y ser nombrado Baker Scholar, entró a trabajar como inversor en Bridgewater, uno de los fondos de alto riesgo más exitosos de la historia.
En sus primeros años, OPA carecía de cualquier estructura corporativa formal. Era una red muy unida de una docena de voluntarios que consideraban a Seb el principal fundador y CEO de facto. La mayoría se encontraban al principio de sus carreras y se habían formado en universidades de élite, con conocimientos que abarcaban las biociencias, la ingeniería, la medicina, el derecho, las finanzas, el espíritu empresarial de las startups, el desarrollo de negocios y las relaciones públicas. Según otros cofundadores de OPA, el hilo conductor era la creencia en la visión de Seb sobre el potencial de la crioconservación... y la voluntad de dedicar voluntariamente enormes cantidades de tiempo a OPA mientras mantenían exigentes empleos a tiempo completo.
Al final, Seb dejó su carrera como inversor para repartir su tiempo entre OPA y otras empresas con una misión relacionada con la crioconservación. Entonces, un voluntario de OPA, Jedd Lewis, se acercó a Seb con una oferta: dejaría sus estudios de doctorado en Stanford, donde había estado realizando investigaciones sobre crioconservación, para ayudar a Seb a recaudar fondos y convertir OPA en una organización sin ánimo de lucro de pleno derecho y dotada de personal. Jedd se había graduado recientemente en la Facultad de Derecho de Harvard y había emprendido una segunda carrera como investigador científico. Se había incorporado mucho después del programa de la NASA que había dado origen a OPA, pero sus aspiraciones eran similares a las de Seb y los demás: por todos los medios, ayudar a aprovechar la naturaleza acelerada del cambio tecnológico para hacer el mayor impacto posible en la salud humana.
"No teníamos ningún plan real de sostenibilidad ni recursos, literalmente un balance negativo", me dijo Jedd. "Pero después de trabajar como voluntario con Seb durante un año vi los resultados que estaba obteniendo. Hizo cosas que yo no había pensado que fueran posibles antes. Cambió por completo mi modelo de cómo alguien podía marcar la diferencia en un área de la ciencia. A día de hoy pienso que podría haber pasado décadas sin aprender esas cosas, y me pregunto cuánto menos impacto habría hecho si nunca hubiera conocido a Seb. Así que nuestro camino estaba despejado. Ambos saltamos sin red de seguridad".
Jedd fue el protegido de Seb durante un año antes de sucederle como CEO de OPA, y Seb permaneció en la junta directiva de OPA durante otro año después. A día de hoy, Seb sigue siendo un voluntario activo y ha donado cientos de miles de dólares a la organización. Jedd le atribuye haber ayudado a hacer posibles muchos de los logros de OPA incluso después de su paso por la dirección de OPA.
OPA y sus asesores sostenían que la convergencia de nuevas tecnologías había hecho de la criopreservación de órganos un reto oportuno. Esta tesis parece haber sido validada por los logros anunciados este mes, que se basaron en avances relativamente recientes en nanotecnología, imagen, 'ómica, modelización computacional e incluso técnica quirúrgica. Con el tiempo, Seb y Jedd reunieron a un nutrido grupo de científicos, cirujanos, médicos, organizaciones científicas y otras partes interesadas que se convencieron de que un esfuerzo de investigación a gran escala en criopreservación debía ser una prioridad máxima de la comunidad científica.
La OPA organizó reuniones científicas en la Casa Blanca, el Capitolio, el programa DARPA del ejército estadounidense, Harvard y Stanford, al tiempo que se asoció con las principales sociedades científicas y médicas para organizar actos destinados a estimular el interés por la crioconservación de órganos. Trabajó con importantes sociedades científicas y médicas, como la Sociedad Americana de Trasplantes y la Asociación de Organizaciones de Obtención de Órganos, para establecer nuevos programas de apoyo a la crioconservación de órganos y tejidos. Su trabajo ha sido ampliamente cubierto en Forbes, así como en The Economist, WIRED, BBC y Scientific American.
OPA se asoció con estas organizaciones y otros líderes de opinión clave para publicar documentos de posición, incluyendo un artículo revisado por pares en Nature Biotechnology que esboza la necesidad de un esfuerzo de investigación en criopreservación de órganos. El artículo fue coescrito con todas las principales sociedades de trasplantes de EE.UU. y un elenco estelar de científicos entre los que se encontraban Robert Langer, George Church y Ed Boyden, e incluso el economista ganador del Premio Nobel Alvin Roth - cuyo trabajo se ha centrado en encontrar nuevas formas de paliar la escasez de órganos. Actualmente se encuentra entre el 1% de los artículos científicos más leídos publicados desde su publicación.
El trabajo de OPA se ha centrado en gran medida en atraer financiación al campo para estimular la investigación en criopreservación de órganos. Muy pronto, OPA persuadió al Departamento de Defensa para que respaldara la investigación en criopreservación con una financiación inicial de 15 millones de dólares. Más tarde trabajó con investigadores y organizaciones interesadas para ayudar a persuadir a la Fundación Nacional de la Ciencia de que lanzara su programa nacional de crioconservación ATP-Bio, reuniendo a un consorcio industrial que incluía a firmes partidarios de la OPO.
Con cinco de estas OPO, OPA creó el Instituto de Investigación Biostasis, un fondo filantrópico privado que apoya la investigación en criopreservación, incluido el estudio sin precedentes sobre criopreservación renal publicado este mes. La propia OPA consiguió financiación de la Fundación Nacional de la Ciencia, el Departamento de Defensa de Estados Unidos, varias organizaciones sin ánimo de lucro centradas en la salud y la longevidad, el Fondo Pineapple y filántropos privados entre los que se encuentran los famosos inversores Peter Thiel y Joe Lonsdale, y el cofundador de Skype Jaan Tallinn. Por el camino, OPA ayudó a los investigadores a mantener un ritmo constante de solicitudes de subvenciones iniciadas por investigadores que aprovechaban la información y los argumentos que OPA había reunido sobre la necesidad de las tecnologías.
Hoy parece que la OPA ha conseguido hacer valer los argumentos a favor de la crioconservación de órganos y tejidos. Tanto el gobierno estadounidense como los inversores de riesgo están empezando a inyectar fondos reales en este campo floreciente. Seb calcula que se han comprometido aproximadamente 300 millones de dólares en los últimos años, y es probable que se obtengan otros 150 millones de dólares de financiación complementaria de fuentes ya existentes si los actuales proyectos de I+D siguen su curso.
El noveno órgano donante
Cuando formuló el OPA allá por 2012 en el campus de la NASA, Seb había empezado a seguir los pasos de los anteriores avances en criopreservación. ¿Qué tipos de seres vivos podían ya criogenizarse? Embriones, ovocitos (óvulos), líneas celulares para investigación... sangre de cordón umbilical... médula ósea. Resultó que la médula ósea humana ya podía crioconservarse y trasplantarse, al menos de donantes vivos.
La médula ósea de donantes salva vidas en muchos tipos de cáncer de la sangre y en una variedad de otras enfermedades sanguíneas. Desde la década de 1950 se han realizado con éxito trasplantes de médula ósea, pero el reto consiste en encontrar una fuente de médula ósea para trasplantar, sobre todo porque donantes y receptores deben ser compatibles por factores genéticos de forma aún más precisa que en algunos trasplantes de órganos.
Los donantes dispuestos se inscriben en un registro de donantes vivos. Cuando una paciente se ve en la necesidad de un trasplante de médula ósea, se busca en el registro donantes compatibles y se les pide que acudan a hacer una donación. Las probabilidades de encontrar un donante potencialmente compatible dependen en gran medida del origen étnico de la paciente que lo necesita. En EE.UU., los pacientes blancos tienen un 79% de posibilidades de encontrar un donante potencialmente compatible. Los pacientes negros o afroamericanos, que tienen una reserva mucho menor de donantes estrechamente compatibles, sólo tienen un 29% de posibilidades de encontrar un posible donante compatible. Incluso cuando se encuentra un posible donante compatible, el método de registro en vida dista mucho de ser una garantía. En todas las edades y etnias, aproximadamente la mitad de los pacientes que lo necesitan fallecen antes de recibir una donación del registro.
Un ejemplo bien conocido es el caso de la Dra. Nalini Ambady, profesora de Stanford a la que se diagnosticó leucemia. Lo más probable es que un trasplante de médula ósea le hubiera salvado la vida, y su familia y amigos llevaron a cabo una búsqueda mundial de un donante. Encontraron al menos seis compatibles lo suficientemente cercanos como para permitir el procedimiento. Todos se echaron atrás tras aceptar inicialmente donar. En 2013, tras un año de intentos fallidos, la Dra. Ambady murió. Solo tenía 54 años.
Seb tropezó con una pregunta que ya se habían planteado otras personas del sector: si la médula ósea podía almacenarse criogénicamente, ¿por qué no obtenerla de donantes de órganos fallecidos que ya estaban proporcionando corazones, hígados y otros órganos para trasplantes? Cada año hay cerca de 40.000 donantes de este tipo en todo el mundo, y cada uno de ellos podría donar potencialmente médula suficiente para varios pacientes que la necesitaran. Para muchos pacientes, cuando se necesitara un trasplante la médula ósea compatible ya estaría disponible en el banco de médula ósea.
Desde la perspectiva del donante de órganos fallecido y de las OPO, esto sería como ofrecer la oportunidad de donar un órgano adicional para salvar vidas. Tradicionalmente, cada donante puede aportar hasta ocho órganos vitales que salvan vidas: un corazón, dos pulmones, dos riñones, un hígado, intestinos y un páncreas. En esencia, la médula ósea sería el noveno. Y si un donante pudiera proporcionar médula ósea a múltiples receptores, esto podría incluso duplicar el número de vidas que cada donante podría salvar.
A finales de 2013, Seb conoció a Louie Helm, ingeniero de software y director adjunto del Instituto de Investigación de Inteligencia Artificial ("MIRI"). El trabajo diario de Louie en el MIRI se centraba en el entonces naciente campo de la seguridad de la inteligencia artificial (I.A.). Más de dos décadas antes de que el auge del ChatGPT impulsara a más de 300 líderes en el campo de la I.A. a identificar el potencial mal uso de la I.A. como un grave riesgo existencial para la humanidad, el MIRI publicaba estrategias para mitigar estos riesgos y desarrollar la I.A. de forma responsable. Los otros intereses de Louie en el campo de la tecnología eran amplios y con una visión de futuro similar. Tras debatir con Seb y otras personas sobre los bancos de médula ósea, Louie publicó en su blog un artículo provocador y lleno de datos titulado "Podríamos criopreservar la médula ósea de los donantes de órganos, pero no lo hacemos". Seb y Louie se propusieron cambiar eso.
A principios de 2015, Seb y Louie obtuvieron el dominio web OssiumHealth.com y formaron Ossium, Inc. con Seb como CEO fundador, con el objetivo de establecer un banco mundial de médula ósea procedente de donantes de órganos fallecidos. En 2016 se formó Ossium Health, Inc. para llevar adelante las actividades y Louie pasó a desempeñar un papel de asesor. Para ayudar a crear Ossium, Seb se dirigió a dos investigadores muy conocidos en el campo del trasplante de órganos que habían publicado experimentos fundacionales que habían ayudado a sentar las bases de Ossium: El profesor Gerald Brandacher de la Johns Hopkins, que había realizado estudios fundacionales recuperando médula ósea de donantes de órganos fallecidos, y el profesor David Sachs de la Universidad de Columbia, la Facultad de Medicina de Harvard y el Hospital General de Massachusetts, que había realizado trasplantes de médula ósea clínicamente.

El Dr. Sachs era conocido sobre todo por haber descubierto muchos de los "HLA" del cuerpo humano, que el organismo de un receptor de trasplantes utiliza para determinar si acepta o rechaza el órgano o la médula ósea de un donante. Durante las décadas anteriores fue responsable de gran parte de los avances en la inducción de tolerancia inmunológica (terapias para convencer al organismo de un receptor de que acepte un órgano donado sin necesidad de una inmunosupresión perjudicial) y los xenotrasplantes (ingeniería genética de órganos animales que pueden trasplantarse a humanos). Más o menos en la época en que Seb se puso en contacto con él, el Dr. Sachs fue galardonado con el Premio Medawar por este trabajo, el máximo galardón a las contribuciones en el campo de los trasplantes.
El Dr. Sachs había realizado estudios clínicos que combinaban el trasplante de un riñón con el de médula ósea del mismo donante. Milagrosamente, este procedimiento permitió a los receptores de trasplantes de riñón vivir sin complicaciones y sin ningún tipo de inmunosupresión, lo que durante mucho tiempo se consideró el santo grial en el campo de los trasplantes. Ossium podría hacer posible este procedimiento para un número mucho mayor de pacientes.
Poco después, Ossium se asoció con AlloSource, uno de los principales proveedores mundiales de tejidos para trasplantes procedentes de donantes de órganos, y también reclutó a otros dos cofundadores: El Dr. Erik Woods, un conocido criobiólogo que había trabajado en métodos para almacenar células madre similares a las del banco de médula ósea de Ossium, y Kevin Caldwell, un joven consultor de gestión de la prestigiosa firma McKinsey & Co. que había trabajado en un equipo que Seb había ayudado a dirigir en el fondo de cobertura Bridgewater. Erik y Kevin dirigen hoy la empresa.
En los años transcurridos desde su creación, Ossium se ha asociado con cerca de la mitad de las OPO de EE.UU. y ha anunciado múltiples ensayos clínicos, incluida la autorización por parte de la FDA de varias solicitudes de nuevos fármacos en investigación (IND) con productos de Ossium. También se ha asociado con el Programa Nacional de Donación de Médula Ósea ("NMDP"), que gestiona el mayor registro de donantes vivos del mundo, para ayudar a hacer llegar su médula ósea a los pacientes que buscan un donante compatible. Ha recibido financiación de diferentes agencias científicas estadounidenses, así como de algunas de las empresas de capital riesgo más prestigiosas del mundo (entre los inversores más destacados se encuentran First Round Capital, General Catalyst, Vivo Capital y Village Global).
El Dr. Brandacher, el Dr. Sachs y Seb han abandonado la empresa, pero en su cátedra el Dr. Brandacher mantuvo una colaboración de investigación con Ossium. Las publicaciones revisadas por pares resultantes dan una idea de lo que el banco de médula ósea podría ser capaz de lograr en el futuro. Entre los nuevos descubrimientos se encuentra un novedoso uso del banco de médula ósea como fuente de células madre mesenquimales ("MSC"). Las CMM tienen un valor terapéutico potencial conocido o sospechado en una enorme variedad de afecciones más allá de las que el banco de médula ósea estaba destinado a tratar en un principio: infartos, Alzheimer y otras enfermedades neurodegenerativas, afecciones autoinmunes e insuficiencia hepática y renal, por nombrar algunas. El Dr. Brandacher y los investigadores de Ossium han informado de que las CMM pueden recogerse del tejido recuperado por Ossium en órdenes de magnitud de mayor abundancia que las fuentes tradicionales.

Con aproximadamente la mitad de las OPO de EE.UU. asociadas ahora con Ossium para facilitar la donación de este "noveno órgano donante" y los principales inversores financiando el esfuerzo, el potencial de salvar vidas de cada donante de órganos parece estar en vías de crecer mucho más. Un solo donante podría resultar capaz de salvar o mejorar la vida de docenas de pacientes de lo que se pensaba hasta ahora... tal vez incluso con un impacto en la salud humana a la par que todos los demás trasplantes de órganos juntos.
Soluciones rápidas a la escasez de órganos
En los primeros días de OPA, Seb y sus compañeros voluntarios visitaron el laboratorio del profesor Mehmet Toner en el Hospital General de Massachusetts ("Mass General"). El Mass General es el hospital insignia del sistema de la Facultad de Medicina de Harvard y un gigante de la investigación biomédica por derecho propio. Mehmet respira un aire enrarecido incluso entre los profesores de allí, ya que publica con regularidad en revistas de primer nivel como Nature y Science. Una de sus mayores fuentes de fama es como pionero en la detección precoz del cáncer.
En 2011 Johnson & Johnson dio a Mehmet y a sus colaboradores 30 millones de dólares para desarrollar una tecnología de biopsia líquida que habían inventado para diagnosticar el cáncer en muestras de sangre. Mehmet y sus colegas utilizaron esto para dirigir un programa de I+D al estilo de la industria dentro del hospital de investigación, que finalmente dio lugar a múltiples empresas de biotecnología. Durante las décadas anteriores a la OPA, Mehmet también había contribuido a que el campo de la crioconservación de tejidos siguiera avanzando, en una época en la que había poca financiación disponible en este campo y pocos científicos serios lo consideraban lo suficientemente interesante o abordable como para trabajar en él. Muchos de los principales investigadores actuales en criopreservación iniciaron sus carreras en el laboratorio Toner.
Mehmet y su protegido en el Mass General, el profesor Korkut Uygun, trabajaban en un enfoque intrigante de la crioconservación de órganos. En lugar de enfrentarse a todo el reto de alcanzar temperaturas criogénicas profundas (por debajo de -140℃) para permitir duraciones ilimitadas de almacenamiento de órganos, Uygun y Toner desarrollaron métodos para enfriar el órgano de forma segura a temperaturas relativamente "altas" por debajo de la congelación. En 2014 enfriaron hígados de rata a -6℃ y los almacenaron durante 3 días antes de trasplantarlos. El procedimiento funcionó en el 100% de las ratas, y los resultados se publicaron en Nature Medicine.
En gran parte, esto funciona para los órganos trasplantados por las mismas razones por las que funciona para los alimentos de su frigorífico: el frío ralentiza el movimiento molecular y reduce la velocidad de las reacciones químicas. Bajar la temperatura amplía la ventana de tiempo antes de que se produzcan lesiones irreversibles y el órgano empiece a deteriorarse. A efectos prácticos, las temperaturas criogénicas profundas (por debajo de unos -140℃) detienen todo movimiento molecular dentro del órgano, lo que equivale a haber "detenido" el tiempo biológico. Pero Toner y Uygun se habían fijado un objetivo más fácil: hacer que el tiempo biológico se moviera más lentamente que nunca, de forma segura y controlada.
Mehmet quería saber si Seb estaría dispuesto a crear una empresa de biotecnología para comercializar la investigación. No era poco pedir: Seb ya estaba trabajando para crear un banco de médula ósea desde cero, y el futuro de la incipiente OPA (en ese momento todavía un grupo de defensa informal) estaba lejos de ser seguro. Por otro lado, este enfoque de "alta temperatura de subcongelación" podría ser exactamente lo que Seb había estado buscando: la vía científica más rápida para eliminar al menos la mayor parte del Talón de Aquiles del sistema de trasplantes. Incluso tiempos de conservación de unos pocos días ampliarían enormemente las opciones de trasplante de cada órgano donado. Si esta investigación pudiera acelerarse aunque sólo fuera unos pocos años, podría significar salvar la vida de muchos miles de pacientes.

Resultó que otro renombrado investigador de la crioconservación había estado dando vueltas a la misma solución: El Dr. Michael Taylor ("Mike" para abreviar). En el campo de la criobiología, Mike era uno de los pocos científicos que trabajaban en el almacenamiento criogénico profundo de tejidos vivos incluso antes del auge de la OPA. Más de una década antes, Mike y otro conocido investigador del campo, el Dr. Kelvin Brockbank, habían hecho un avance crítico en la crioconservación: habían demostrado la primera vitrificación (crioconservación sin hielo) de un tejido sólido de gran tamaño con función y éxito de trasplante tras su almacenamiento a temperaturas criogénicas profundas (por debajo de -140℃), lo que hacía posible el estreno de sistemas vivos más grandes como los órganos para trasplante y ayudaba a sentar las bases del esfuerzo de investigación catalizado posteriormente por la OPA. Los resultados se publicaron en la preeminente revista de bioingeniería Nature Biotechnology. Pero mucho antes de ayudar a descubrir cómo los órganos y los tejidos pueden sobrevivir a la congelación, Mike había experimentado con enfoques para llevar los órganos de forma segura a las mismas "altas" temperaturas bajo cero que los investigadores del Mass General tenían ahora en su punto de mira.
En el campo de los trasplantes Mike era más conocido como uno de los desarrolladores del transportador de riñones LifePort. Durante muchos años, el LifePort había sido el dispositivo líder del mercado para preservar los riñones mientras eran transportados de los donantes a los receptores. Fue el primero de una nueva generación de dispositivos para perfundir los órganos de los donantes antes del trasplante: mientras que tradicionalmente los órganos trasplantados se colocaban simplemente en un lecho de hielo y se llevaban a toda prisa del donante al receptor, el LifePort proporcionaba una especie de sistema circulatorio artificial. Suministraba un sustituto sanguíneo a la propia vasculatura del órgano, lleno de medicamentos y conservantes para mantenerlo sano durante todo el trayecto.
El LifePort había dado el pistoletazo de salida a un cambio sísmico en el trasplante de órganos que aún se está produciendo hoy en día. Cada vez se perfunden más corazones, pulmones, hígados y riñones trasplantados después de recuperarlos del cuerpo del donante para imitar el entorno natural del órgano. Esto permite a las OPO y a los equipos de trasplante recopilar datos sobre la salud y la función del órgano, lo que permite predecir mejor su posible rendimiento en el cuerpo del receptor. En la actualidad se comercializan o están en fase de ensayo clínico muchos dispositivos diferentes. Éstos han desempeñado un papel importante en el espectacular aumento de los trasplantes de órganos en la última década: han sido ampliamente adoptados en Europa, y su adopción también ha aumentado de forma constante en EE.UU. a pesar de que el proceso de aprobación reglamentaria del país es más lento.
Estas plataformas son populares en gran medida porque pueden resolver muchas de las preocupaciones que puede tener un equipo de trasplantes sobre si el órgano funcionará lo suficientemente bien como para merecer ser trasplantado a su paciente. Mientras que el aumento de los tiempos de preservación puede permitir ofrecer órganos a más centros, la perfusión de órganos puede permitir que más de esos centros digan "Sí" a cada oferta.
Continúe leyendo la nota en Forbes US.

 Yahoo Finanzas
Yahoo Finanzas 